Функционалните групи на органични съединения
Функционални групи са групи от атоми, които предизвикват специфични химични свойства на този клас вещества.


Като се има предвид полярността на О-Н и значителен положителен заряд на водороден атом, споменатият водород е хидроксилна група има "кисел" характер. Поради това той рязко различни от водородни атоми, съдържащи се в въглеводород радикал. кислородния атом на хидроксилната група е с частичен отрицателен заряд и две несподелени електронни двойки, което позволява молекулите на алкохол образуват водородни връзки.

Чрез химични свойства, различни от алкохоли с феноли, което се причинява от взаимното влияние в молекулата на фенол хидроксилна група и бензеновия пръстен (фенил - С6 Н5). Този ефект се свежда до факта, че пи-електрони на бензолното ядро включват частично в обхвата си несподелени електронни двойки кислородния атом на хидроксилната група, като по този начин намаляване на плътността на електрони на кислородния атом. Това намаление се компенсира от по-голяма поляризация на О-Н, което от своя страна води до повишаване на положителния заряд на водородния атом:
Следователно, водородът на хидроксилната група в молекулата на фенол има киселинен характер.
Ефектът на атомите в молекули на фенол и неговите производни взаимно. Хидроксилната група има ефект върху плътността на π-електронен облак в бензеновия пръстен. Това намалява при въглеродния атом, свързан с ОН-група (т.е., в мета-позиция на първото и 3 въглеродни атома.) И се издига върху съседни въглеродни атоми - 2, 4, 6-та - орто - и пара позиция.
водородните атоми на бензен и орто по - и пара позиция са по-мобилни и лесно заменени с други атоми и радикали.
Алдехиди с обща формула. където - С = О - карбонилна група. въглероден атом в карбонилната група на SP 2 - хибридизира. Атомите са пряко свързани с него, са в една и съща равнина. Поради големия elektorootritsatelnosti кислородния атом в сравнение с въглеродния атом на С = О връзка е силно поляризиран чрез изместване на плътността на π-електронна поради кислород:

Под влияние на карбонил въглеродния атом на алдехиди до повишена полярност връзка С-Н, което повишава реактивоспособността на Н. атом
карбоксилни киселини

карбоксилни киселини, хидроксилна група свързана към един въглеводороден радикал и карбоксилна група. Затихване връзка между кислород и водород в хидроксилната група се обяснява с разликата в electronegativities на атома въглерод, кислород и водород. въглероден атом придобива някои положителен заряд. Този въглероден атом привлича електрони облакът от кислородни атоми на хидроксилната група. Компенсиране на изместване на електронната плътност, кислороден атом на хидроксилната група да се издърпва електронен облак съседен водороден атом. Съобщение ОН в хидроксилната група е по-полярния, и водороден атом придобива по-голяма мобилност.
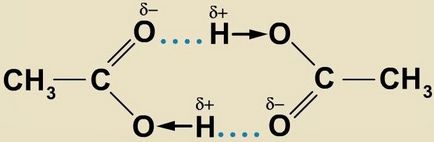
Водородното свързване мед молекули на карбоксилни киселини: