Методи за получаване на водород от вода
Производство на водород като у дома си доста лесен процес и има няколко начина да направите това:
1. Не трябва да се страхуваме от основния разтвор, защото тези имена всичко това е в публичното пространство.
Например, чисти "мол" тръби идеален състав. Излива се в колба и запълване малко алкализира с 100 мл вода;
Смесва се добре да се разтвори кристали;
Добавянето на няколко малки парчета от алуминий;
Чакаме около 3-5 минути, докато реакцията ще се проведе възможно най-бързо;
Добавянето на допълнителни няколко парчета от алуминий и 10-20 грама алкален;
Колбата се затваря със специален резервоар тръба, която води в резервоар за събиране на газ и изчакайте няколко минути, докато въздухът се освобождава под налягане водород от съда.
2. Изолиране на водород от алуминиева сол и меден сулфат.
Колбата се изсипва меден сулфат сол и малко повече;
Всички разрежда с вода и се смесва добре;
Поставете колбата в резервоар за вода, тъй като реакцията ще се разпределят много топлина;
В противен случай, всичко, което трябва да направите, както и в първия метод.
3. Получаване на водород от вода чрез преминаване ток през разтвор 12В сол във вода. Това е най-лесният начин и най-подходящ за домашна обстановка. Единственият недостатък на този метод е, че водородът освободен е относително малък.
И така Сега, че знаете как да се получи водород от вода, и не само. Можете да прекарват много експерименти. Не забравяйте да се придържат към правилата за безопасност, за да се избегнат наранявания.
Производство на водород като у дома си
Тази статия описва най-популярните методи за производство на евтин водород в дома.
Метод 1. водород алуминий и алкали.
Алкално разтвор се използва - калиев хидроксид или натриев хидроксид. Секретираният водород чист, отколкото в киселина реакцията с активни метали.
Излива се в колба малко количество калиев или натриев хидроксид и запълване 50 до 100 мл вода, разтворът се разбърква до пълно разтваряне на кристалите. След това добавете няколко парчета алуминий. Незабавно започва реакцията с отделяне на водород и топлинна енергия, на пръв слаб, но непрекъснато се разраства.
След като изчака реакцията ще бъде по-активен, внимателно се добавят още 10 гр. алкални и някои парче алуминий. Така че ние значително засилване на процеса.
Запушена колба, епруветка с тръбичка, водеща към съд за събиране на газ. Чакаме около 3 до 5 минути. докато водород измества въздуха от съда.
Както водород се получава? филм оксид, който покрива повърхността на алуминий, при контакт с алкален унищожени. Тъй като алуминият е активен метал, той започва да реагира с вода, разтваря се в него, водородът се освобождава.
2AL + 2NaOH + 6h3O → 2Na + 3h3 ↑
Метод 2. водород от алуминий, меден сулфат, и готварска сол.
Колбата се изсипва малко меден сулфат, и техни соли. Добавя се вода и се разбърква докато се разтвори. Разтворът трябва да светне зелено, ако това не се случи, се добавя малко количество сол.
Колбата е необходимо да се поставят в чаша напълнена със студена вода, като реакцията ще се разпределят много топлина.
Добави към разтвора се поставят няколко парчета алуминий. Започва се реакция.
Как е отделянето на водород? Методът произвежда меден хлорид, разтваряне филм оксид с метал. Едновременно с намаляването на мед настъпва образуване на газ.
Метод 3. водород от цинк и солна киселина.
Поставен в тръби цинкови парчета и ги запълни със солна киселина.
Като активен метал цинк чрез взаимодействие с киселина от него измества водород.
Zn + 2HCl → ZnCl2 + h3 ↑
4. Метод на производство на водород чрез електролиза.
Се пропуска през разтвор на вода и сол заварени електрически ток. Когато реакцията се отделя водород и кислород.
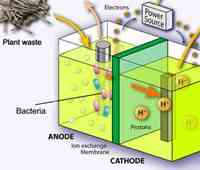
Производство на водород чрез електролиза на вода.

Този модел не е подходящ за висококачествен ежедневна употреба. Но тества идеята се провали. Затова реших да се прилага електродите на графит. Чудесен източник за графитни електроди е текущата количка колектор. Те са пълни с ролки на последната спирка. Ние трябва да помним, че един от електродите ще бъде унищожен.
Нарязване и промяна на даден файл. Интензитетът на електролизата зависи от текущото съдържание и площта на електродите. Към електродите прикрепен проводници. Проводниците трябва да бъдат внимателно изолирани. Жилища електролизер модел трябва да се оправи пластмасови бутилки. Капакът направени отвори за тръби и проводници. Всички внимателно намазана уплътнител.
За свързване на две цистерни годни нарязани на вратовете на бутилки. Те трябва да бъдат свързани заедно и oplavit шев. Ядки от капачки от бутилки. Двете бутилки са изработени в дъното на дупката. Всичко е свързано и внимателно изпълнена с лепило.
Потребителят ще използват мрежата като източник на напрежение 220V. Искам да предупредя, че това е опасна играчка. Така че, ако не разполагат с достатъчно умения или има някакво съмнение, най-добре е да не се повтарят. Домашната мрежа са променлив ток, електролиза, трябва да се изправи. За да направите това, диоден мост се вписват перфектно. Това е, което на снимката не е достатъчно мощен и бързо изгарят. Най-добрият вариант е китайските MB156 диод мост в алуминиево покритие.
Диод мост става много горещо. Това ще трябва активно охлаждане. Cooler за процесора на компютъра се вписва перфектно. За случай, можете да използвате правилния размер raspayachnuyu кутията. Продаден в електрически стоки.
Под диод мост е необходимо да се поставят няколко слоя от картон. Капакът на кутията raspayachnoy направили необходимите отвори. Тук е инсталирането на сбора. Клетката се захранва от мрежата, вентилаторът на универсалната захранването. Разтворът на електролит се използва сода. Тук трябва да се помни, че колкото по-висока концентрацията на разтвора, толкова по-висока скорост на реакция. Но това по-високо и отопление. И това допринася за отоплението на реакцията ще направи разлагането на натрий на катода. Тази реакция е екзотермична. В резултат на това ще произвежда водород и натриев хидроксид.
Апаратурата, че в снимката по-горе, много горещо. То трябваше да бъде периодично включен и изчакайте, докато се охлади. Проблемът с нагряването частично решен чрез охлаждане на електролита. За това се използва помпата за настолен фонтан. Дълга тръба се простира от една бутилка към друг през помпата и кофа студена вода.
Връзка тръба до топката и да се осигури от чешмата. Продаден в магазини за домашни любимци в отдела за аквариуми.
Основни познания за класическата електролиза.
Принципът на ефективността на електролизер за h3 и O2 газ.
Със сигурност всеки знае, ако пропусне два пирона в разтвор на сода за хляб и кандидатства за още един пирон плюс и минус, от друга страна, тя ще се открояват на червения водорода и кислорода в положителна територия.
Сега нашата задача е да се намери подход, за да получите най-много от този газ, и прекарват минимално количество електроенергия.
Урок 1: Напрежение
Водата на разлагане започва, когато се прилага към електродите малко повече от 1.8 волта. Ако приложите 1 волт, на ток почти не излиза и не се открояват газ, но когато напрежението се доближава до стойността от 1,8 волта, токът започва да се покачва рязко. Това се нарича минимален потенциал електрод, при която започва електролиза. Poetomu- ако ние ще предостави 12 волта на 2 нокътя - след като електролизер ще ядат много електричество и газ няма да бъде достатъчно. Цялата енергия ще отиде в загряване на електролита.
Поръчка. в нашия електролизер е икономическа - трябва да се представи не повече от 2 волта на клетка. Ето защо, ако имаме 12 волта - ние ги разделят на 6 клетки и да получите на всяка от 2 волта.
Сега опростяване - просто разделяне на контейнера в 6 части plastinami- Резултатът е шест клетки, свързани в серия е 2 волта всяка вътрешна плоча от едната страна ще бъде плюс за всяка клетка, както и други по-малко. Така че - урок научих = броят 1 нанесете малко напрежение.
Сега втората ефективност урок: Разстоянието между плочите
Колкото по-голямо разстояние - толкова по-голяма съпротива, толкова повече ток ще похарчи за да се получи един литър газ. По-краткият разстоянието - колкото по-малко харчат вата на час на литър газ. Освен това, ще се използва този термин - индекс електролизер ефективност / Графиката показва, че колкото по-близо плаките са заедно - по-малък напрежението, необходима за подаване на същото ток. изход А газ е известно пряко пропорционална на количеството на текущата преминаване през електролита.
Произведението на малък напрежение в ток - ние получаваме по-малко вата за същото количество газ.
Сега третия урок. квадратни плочи
Ако вземем гвоздея 2 и с помощта на първите две правила ги организира в тясно сътрудничество и ще ги представи на 2 волта - газът се много малко, тъй като те ще пропуснат много малко ток. Опитайте при същите условия да се вземат две плочи. Сега сумата на текущия и газ ще се увеличи в пряка зависимост от квадрата на плочите.
Сега четвъртият урок: концентрация на електролита
Използването на първите три правила вземат големи железни плочи в малко разстояние един от друг и те ще осигури 2 волта. И ги спусна в vodichku, добавяйки щипка сода за хляб. Електролиза ще отида, но много бавно, водата ще се загрява. Йони в разтвор е много съпротивление е малък, топлината се намалява и количеството на газ се увеличава
Източници: 505sovetov.ru, all-he.ru, zabatsay.ru хп ---- dtbbgbt6ann0jm3a.xn - p1ai, domashnih-usloviyah.ru